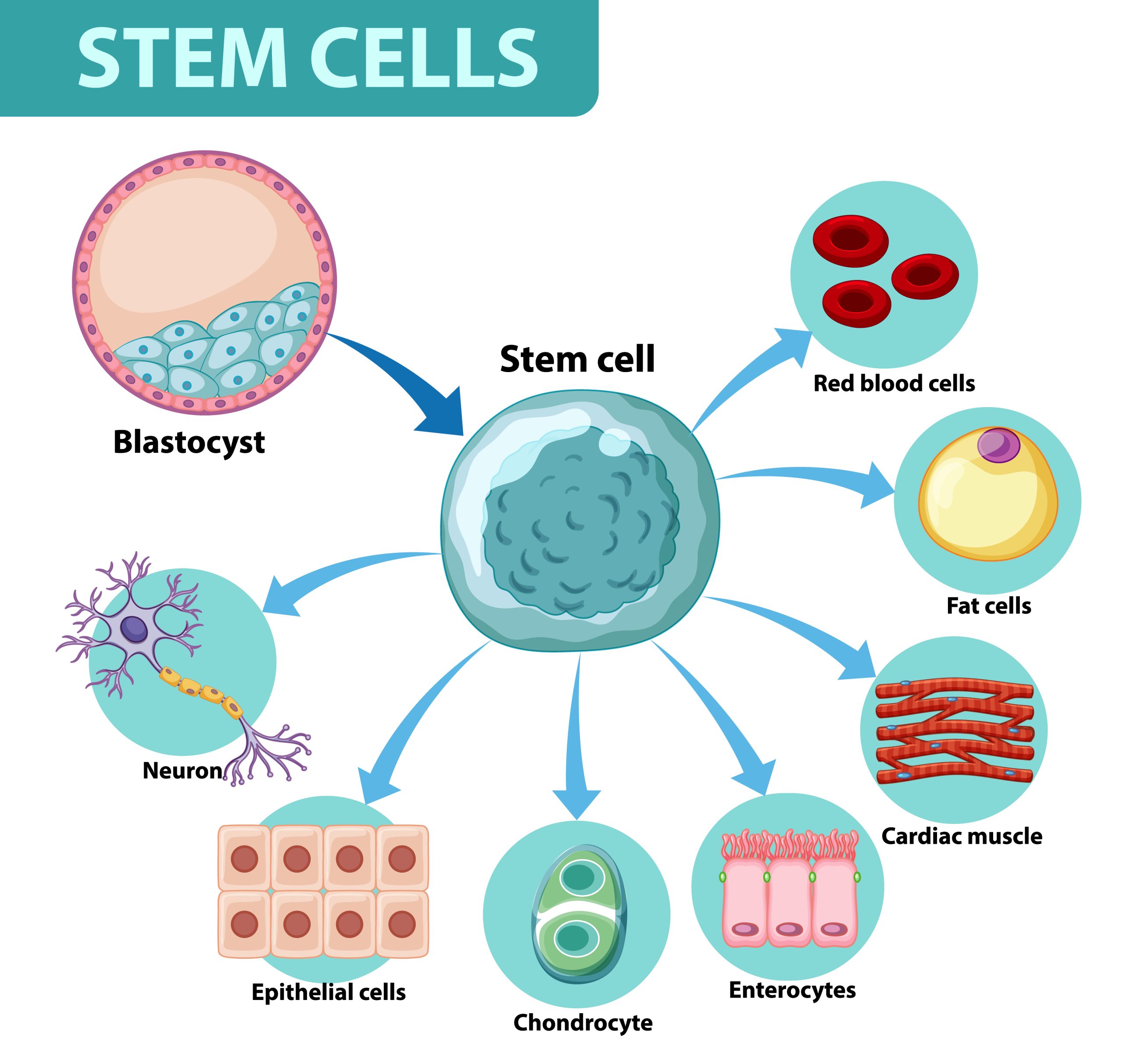
In ultimul deceniu, medicina regenerativa a trecut de la promisiune teoretica la aplicatii reale in spitale, laboratoare si centre de transplant. Punctul central il reprezinta celule stem, capabile sa se auto-reinnoiasca si sa se transforme in diverse linii celulare necesare pentru refacerea tesuturilor. De la primele incercari de transplant medular realizate in anii 1960 pana la terapii avansate combinate cu biomateriale si imprimare 3D, drumul a fost ghidat de progrese stiintifice, standarde de calitate mai stricte si un cadru de reglementare tot mai clar. In cele ce urmeaza, vom vedea concret cum functioneaza aceste mecanisme, ce tipuri celulare sunt folosite, unde exista deja rezultate clinice solide si cum ne asiguram ca siguranta si etica raman pe primul loc.
Perspectiva istorica este esentiala: in 1968 s-a realizat unul dintre primele transplanturi de celule hematopoietice (din maduva osoasa), deschizand calea pentru tratarea leucemiilor si a altor hemopatii maligne. In 1988 a fost raportat primul transplant reusit de sange din cordon ombilical pentru o boala ereditara, aratand ca sursele pot fi variate si mai usor accesibile. Ulterior, in 2006, a aparut o revolutie tehnologica prin reprogramarea celulara (celule pluripotente induse, iPSC), iar in 2012 a fost decernat Premiul Nobel pentru aceasta descoperire, confirmand impactul sau urias. Astazi, organizatii precum OMS (Organizatia Mondiala a Sanatatii), FDA (Agentia pentru Alimente si Medicamente din SUA) si EMA (Agentia Europeana a Medicamentului) sustin ghiduri si reglementari care influenteaza direct felul in care terapiile sunt dezvoltate si aprobate.
Ce inseamna regenerarea tisulara si de ce conteaza acum
Regenerarea tisulara se refera la capacitatea organismului de a reface structuri si functii compromise in urma traumelor, bolilor degenerative sau a interventiilor chirurgicale. Aceasta nu inseamna doar inlocuirea celulelor moarte, ci si refacerea arhitecturii tisulare corecte, a vaselor de sange si a comunicarii dintre celule. In practica, regenerarea eficienta inseamna ca un pacient cu o leziune complexa de cartilaj sa poata reveni la mobilitate fara dureri cronice sau ca un pacient cu arsuri extinse sa-si recupereze un tegument functionaI, elastic si rezistent la infectii.
Interesul crescut din prezent vine din trei directii. Prima este nevoia clinica: populatia imbatraneste, iar bolile degenerative ale articulatiilor, inimii si sistemului nervos sunt in crestere. A doua tine de maturizarea tehnologiilor: culturi celulare standardizate, bioreactoare, testare genetica si instrumente precise pentru controlul calitatii. A treia este aparitia unui cadru de reglementare mai bine definit, precum Regulamentul european pentru terapii avansate (ATMP) din 2007 si instrumente de accelerare a aprobarilor in SUA dupa 2016, care permit ca inovatiile validate sa ajunga mai repede la pacienti, fara compromisuri privind siguranta.
Datele istorice arata clar utilitatea clinica in cel putin un domeniu: hemato-oncologia. Timpul mediu pana la prinderea grefei (engraftment) pentru neutrofile dupa un transplant alogen de celule hematopoietice este frecvent intre 14 si 21 de zile, iar pentru trombocite intre 16 si 28 de zile, valori care ghideaza monitorizarea post-transplant in centrele specializate. In Europa, rapoartele registrului EBMT au consemnat in anul 2019 circa 48.000 de proceduri de transplant de celule hematopoietice intr-un singur an, indicand o infrastructura consistenta si rezultate reproductibile la scara continentala. Aceste repere numerice ne arata ca regenerarea nu mai este doar o idee abstracta, ci un set de procese cu logistica, protocoale si indicatori de performanta masurabili.
Mecanisme celulare si moleculare care sustin refacerea tesuturilor
Capacitatea de refacere a unui tesut depinde de interactiunea fina dintre auto-reinnoirea celulelor, diferentierea lor controlata si un dialog molecular intens cu microambientul. In termeni simpli, trei straturi de mecanisme lucreaza simultan: (1) proliferarea celulelor cu potential inalt, (2) ghidarea lor catre liniile potrivite (osteogena, condrogena, miogena, endoteliala etc.) si (3) remodelarea matricei extracelulare, alaturi de formarea unei microcirculatii functionale. Un rol aparte il au semnalele paracrine: citokine, factori de crestere si vezicule extracelulare (inclusiv exozomi de 30–150 nm) ce reangajeaza celule locale, atenueaza inflamatia si atrag noi vase de sange. Astfel, reparatia nu inseamna doar inlocuire celula-cu-celula, ci si resetarea retelei tisulare.
In plus, populatii precum cele mezenchimale (MSC) pot exercita efecte imunomodulatoare: reduc expresia unor citokine pro-inflamatorii (de ex., TNF-alfa) si cresc eliberarea altora cu rol protector (de ex., IL-10), ceea ce pregateste terenul pentru o refacere ordonata. Fenomenul de homing – migrarea tintita catre locul lezat – este ghidat de axe chemokinice (cum ar fi SDF-1/CXCR4) si de molecule de adeziune. Nu in ultimul rand, diferentierea este orchestrata prin retele de factori de transcriptie (RUNX2 pentru os, SOX9 pentru cartilaj etc.) si prin proprietatile mecanice ale microambientului: substraturi cu modul elastic mai ridicat favorizeaza destinul osteogenic, in timp ce medii mai moi orienteaza spre alte linii.
- 🧭 Chemotaxie si homing: deplasare ghidata de gradienti chemokinici (ex.: SDF-1/CXCR4), cu acumulare locala masurabila in primele 24–72 de ore post-administrare.
- 🧪 Semnalizare paracrina: eliberare de factori (VEGF, HGF, IGF-1) si exozomi (30–150 nm) ce reduc inflamatia si favorizeaza angiogeneza.
- 🧱 Remodelare a matricei: secretie de MMP-uri si integrine care regleaza adeziunea si reorganizarea fibrelor de colagen.
- 🔧 Mecanotransductie: sensibilitate la rigiditatea substratului (de ordinul kPa pana la zeci de kPa), influentand expresia genica si destinul celular.
- 🧯 Imunomodulare: scaderea TNF-alfa/IFN-gamma si cresterea IL-10/TGF-beta in anumite contexte, cu efecte masurabile asupra edemului si durerii.
- 🧩 Diferentiere ghidata: activarea factorilor cheie (RUNX2, SOX9, MYOD) si a cailor Wnt/Notch/TGF-beta in functie de tesutul tinta.
Aceste mecanisme converg catre un obiectiv comun: restabilirea functiei. In testele preclinice, de pilda, se folosesc frecvent densitati de insamantare intre 1 si 10 milioane de celule pe mililitru de hidrogel pentru a obtine depozite omogene, iar in constructiile osoase se tintesc porozitati si diametre de pori in intervalul 100–400 micrometri pentru a balansa rezistenta mecanica si invazia vasculara. La nivel clinic, monitorizarea include biologie (markeri inflamatori, factori de crestere), imagistica (RMN, CT) si scoruri functionale validate, pentru a lega dinamica celulara de recuperarea perceputa de pacient.
Surse si tipuri: HSC, MSC, iPSC si celule adulte
Sursele principale utilizate in regenerare pot fi grupate in patru categorii operative. In primul rand, celulele hematopoietice (HSC) din maduva osoasa, sange periferic mobilizat sau sange de cordon ombilical, sunt standardul de aur pentru reconstituirea sistemului hematopoietic. In practica, doza tinta de celule CD34+ in transplanturile autologe se situeaza adesea intre 2 si 5 x 10^6 celule/kg, prag corelat cu o prindere mai rapida a grefei. In al doilea rand, populatiile mezenchimale (MSC) izolate din maduva, tesut adipos, cordon sau alte surse stromale, care au capacitati de diferentiere tri-linie (os, cartilaj, adipocite) si efecte paracrine/antiinflamatorii valoroase. In al treilea rand, populatiile tisulare adulte specializate (de ex., celule satelit musculare, celule din straturile bazale epidermice) ce contribuie la intretinerea locala a tesuturilor. In al patrulea rand, iPSC – celule pluripotente induse prin reprogramare, descrise in 2006 si aduse in prim-planul cercetarii mondiale prin Premiul Nobel 2012 – care pot, in principiu, sa genereze aproape orice tip celular somatic.
Pentru MSC, International Society for Cell & Gene Therapy (ISCT) a propus criterii minimale de identificare inca din 2006, utilizate pe scara larga: adeziune la plastic in conditii standard, expresie pozitiva a markerilor CD73, CD90 si CD105 (>95%) si lipsa expresiei CD14, CD34, CD45, CD11b, CD19 si HLA-DR (70%) si teste microbiologice, inainte de a ajunge in clinica.
- 🧬 HSC: reconstituie hematopoieza; doze uzuale 2–5 x 10^6 CD34+/kg; engraftment neutrofilic adesea la 14–21 zile.
- 🧫 MSC: efecte paracrine si imunomodulare; criterii ISCT (CD73/CD90/CD105 >95%; markeri hematopoietici negativi <2%).
- 🧠 iPSC: obtinute prin reprogramare (2006), pluripotente; utile pentru modelare de boala, screening de medicamente si potentiale terapii personalizate.
- 🧴 Celule adulte specializate: prezente in tesuturi ca rezerve locale (epiderma, muschi, ficat), cu rol in mentenanta si reparatie.
- 🧪 Calitate si siguranta: viabilitate >70%, testare sterilitatii, evaluare genetica (cariotip stabil) pentru a limita riscurile.
Alegerea sursei depinde de obiectiv. Pentru revascularizare locala si control al inflamatiei, MSC pot fi preferate; pentru boli ale sangelui, HSC sunt standard; pentru necesitati de substitutie la scara mare (de ex., foite epiteliale pentru arsuri), celulele epiteliale autologe expandate ex vivo sunt dovedite; iar pentru linii greu accesibile (de ex., neuroni dopaminergici), iPSC ofera o cale scalabila. Logistica este, de asemenea, decisiva: recoltarea din cordon ombilical este unica si neriscanta pentru mama si copil (o singura ocazie la nastere), in timp ce recoltarea de tesut adipos poate fi repetata la adult. In toate cazurile, criteriile cantitative si calitative raman piatra de temelie pentru a transforma potentialul biologic intr-o terapie reproductibila.
Aplicatii clinice: de la sange la piele, cartilaj, cornee si cord
Exista domenii unde rezultatele sunt bine consolidate si altele in care dovezile sunt promitatoare dar inca matura. In hemato-oncologie, transplantul de celule hematopoietice este tratament standard pentru multiple tipuri de leucemie si limfoame. In 2019, registrul european EBMT a raportat aproximativ 48.000 de astfel de proceduri realizate intr-un singur an in Europa, o cifra ce reflecta atat prevalenta indicatiilor, cat si maturitatea lantului de aprovizionare (donatori, tipare HLA, crioconservare, centre acreditate). Timpii medii de prindere a grefei, monitorizarea citopeniilor si consumul de produse sanguine sunt azi bine cuantificate, ceea ce permite comparatii intre protocoale si centre.
In arsuri severe, folosirea foitelor epiteliale autologe crescute in cultura a fost descrisa inca din anii 1980, reducand mortalitatea si riscul de infectii in cazurile extinse. Ratele de integrare (“take rate”) pot depasi 70% in centre cu experienta, iar reducerea suprafetei de autogrefare scade trauma donatoare si timpul total de spitalizare. In oftalmologie, utilizarea celulelor limbare pentru a reface suprafata oculara in deficitele limbare a fost dusa pana la produse autorizate in Uniunea Europeana in 2015, aducand pentru pacienti imbunatatiri obiective ale acuitatii vizuale si reduceri ale durerii si fotofobiei.
In ortopedie, reparatia leziunilor condrale prin tehnici de tip ACI (autologous chondrocyte implantation), raportata initial in 1994, a trecut prin mai multe generatii tehnologice, integrand ulterior biomatrice si, in unele protocoale, populatii stromale pentru a creste calitatea cartilajului neoformat. Parametri standardizati, precum scorurile ICRS la 12–24 luni, permit cuantificarea rezultatelor si comparatia intre dispozitive si strategii. In cardiologie, studiile timpurii din anii 2000 cu celule progenitoare injectate in miocard dupa infarct au aratat imbunatatiri modeste ale fractiei de ejectie (adesea in ordinul a 3–5 puncte procentuale in meta-analize timpurii), dar lectiile invatate au orientat campul catre livrare mai precisa, selectie celulara mai potrivita si combinatii cu hidrogeluri pentru retentie crescuta in miocard.
- 🏥 Transplant HSC: ~48.000 proceduri in Europa in 2019; timpi tipici de engraftment 14–21 zile (neutrofile), 16–28 zile (trombocite).
- 🔥 Arsuri: foite epiteliale autologe in uz clinic de zeci de ani; rate de integrare adesea >70% in centre cu experienta.
- 👁️ Suprafata oculara: terapii derivate din celule limbare, cu produse autorizate in UE din 2015 pentru deficite limbare.
- 🦴 Cartilaj: ACI introdus in 1994; evaluari ICRS la 12–24 luni arata ameliorari functionale si structurale.
- ❤️ Inima: imbunatatiri modeste (3–5 pp) ale LVEF in studiile timpurii; accent actual pe retentie, selectie celulara si biomateriale.
Este important de subliniat ca nu toate indicatiile sunt la acelasi nivel de dovada. Pentru unele patologii neurologice sau autoimune, dovezile raman neconcludente ori limitate la faze I/II, iar autoritatile solicita date robuste de eficacitate si siguranta pe termen lung. Tocmai de aceea, colaborarea cu registre clinice, standardizarea masuratorilor (inclusiv imagistica cuantitativa si scoruri validate) si transparenta rezultatelor negative sunt esentiale pentru a transforma cazurile promitatoare in standarde terapeutice de maine.
Inginerie tisulara si biomateriale: cum se construieste un tesut functional
Regenerarea durabila presupune nu doar celule potrivite, ci si un “schelet” tridimensional si un microambient care sa le ghideze. Biomaterialele – de la colagen si gelatina, la alginat, hialuronat, chitosan sau polimeri sintetici precum PLGA si PCL – pot fi proiectate cu proprietati mecanice si de degradare adaptate tesutului tinta. De exemplu, pentru os, se prefera structuri cu rigiditate mai mare si porozitate interconectata (100–400 micrometri) pentru a permite invazia vasculara si depozitarea rapida a matricei minerale; pentru cartilaj, se cauta elastomeri hidratati cu modul elastic mai redus, care sa mimeze proprietatile condrocitelor si ale matricei bogate in proteoglicani.
In ultimele doua decenii, imprimarea 3D si bioprintarea au permis aranjarea spatiala precisa a celulelor si materialelor, in stratificari ce reproduc zonele anatomice (de ex., strat superficial, zona de tranzitie si strat profund pentru cartilajul articular). Bioreactoarele adauga stimuli mecanici si flux controlat de nutrienti/oxigen pentru a favoriza maturarea grefei inainte de implantare. Din punct de vedere cantitativ, densitatile de insamantare se situeaza adesea intre 1 si 10 milioane de celule/mL, iar difuzia oxigenului devine critica peste ~200 micrometri grosime a stratului celular, motiv pentru care se introduc canale microvasculare sau se folosesc factori pro-angiogenici (precum VEGF) pentru a grabi vascularizarea post-implant.
- 🧱 Arhitectura: porozitate si diametru al porilor (100–400 µm pentru os) pentru echilibru intre rezistenta si invazia vasculara.
- ⚖️ Mecanica: modulul elastic ajustat tesutului tinta (kPa pentru cartilaj, zeci–sute de MPa pentru substituenti osoasi compoziti).
- 🧯 Bioactivitate: incorporare de peptide adezive (ex.: RGD) si factori de crestere in doze controlate (ng–µg per dispozitiv).
- 💧 Transport: grosime a constructului si canale de perfuzie pentru a depasi limita de difuzie (~200 µm fara vascularizare).
- 🧫 Insamantare: 1–10 milioane celule/mL in hidrogeluri; distributie omogena pentru evitare de zone necrotice.
- 🧲 Bioprintare: pattern-uri multi-material si co-culturi (ex.: endoteliale + stromale) pentru retele vasculare mai rapide.
La interfata cu organul gazda, interactiunile sunt dictate de proteinele adsorbite, topografia la scara nano si micro si dinamica degradarii. Daca un material se degradeaza prea repede, nu ofera suport suficient pentru depozitarea matricei; daca se degradeaza prea incet, poate limita integrarea si induce raspunsuri inflamatorii cronice. In clinica, parametri precum stabilitatea mecanica la 6–12 luni, gradul de integrare masurat imagistic si scorurile functionale validate (IKDC, KOOS, AOFAS etc.) devin jaloane cantitative pentru a spune daca o grefa este cu adevarat “regenerativa” si nu doar un inlocuitor pasiv. Combinatia potrivita intre tipul celular, designul biomaterialului si o livrare precisa face diferenta intre o solutie eleganta in laborator si un rezultat robust pentru pacient.
Reglementare, standarde si siguranta: cum ne asiguram de calitate
Faptul ca discutam despre terapii vii inseamna ca siguranta, calitatea si trasabilitatea sunt critice. In Uniunea Europeana, din 2007 exista cadrul pentru Terapii Avansate (ATMP), care include terapiile celulare, terapia genica si produsele de inginerie tisulara. In Statele Unite, Legea din 2016 a introdus designari accelerate pentru terapiile regenerative (de tip RMAT), iar din 2017 FDA a publicat un pachet de ghiduri menite sa clarifice cand o interventie este considerata manipulare minima sau necesita autorizare completa ca medicament/tip de produs biologic. Aceste repere, coroborate cu standarde GMP (Good Manufacturing Practice) si cu cerinte ferme pentru studii clinice, stabilesc coloana vertebrala a sigurantei.
La nivel profesional, ISCT a stabilit criterii minimale pentru identificarea MSC in 2006, adoptate pe scara larga. Parametri cuantificabili – de pilda, expresie pozitiva >95% pentru CD73/CD90/CD105 si negative <2% pentru markeri hematopoietici/HLA-DR – au devenit limbaj comun in dosarele de dezvoltare. In paralel, cerintele uzuale pentru eliberarea unui lot includ viabilitate celulara peste 70%, absenta contaminarii microbiene si profil genetic stabil (cariotip normal), reduceand riscul de transformare sau anomalii cromozomiale. Trasabilitatea – de la donator la produsul final si pana la pacient – este documentata riguros, cu timpi limite pentru procesare (adesea 24–72 de ore pentru anumite produse proaspete) si validari ale crioconservarii (rata de racire, crioprotectori precum DMSO la 5–10%).
Organizatii internationale precum OMS sustin retelele nationale pentru sange si transplant, incurajeaza hemovigilenta si elaboreaza recomandari pentru calitate si siguranta. In practica, centrele acreditate raporteaza evenimente adverse, iar autoritatile reevalueaza balanta risc–beneficiu pe masura ce se acumuleaza date. Un aspect sensibil il reprezinta ofertele comerciale nereglementate: clinici care promit solutii pentru aproape orice afectiune, fara dovezi reale. Diferenta intre o terapie aprobata si una nereglementata sta adesea in cifrele pe care le-am mentionat: doze definite, markeri acceptati, criterii de includere/excludere, endpoints obiective si urmarire pe termen lung (12, 24, 36 de luni sau mai mult).
In final, siguranta inseamna si selectie atenta a indicatiei. Chiar daca o populatie celulara are proprietati remarcabile in laborator, eficacitatea clinica depinde de livrare (loc, volum, concentrare), de microambientul receptor si de patologia de baza. Acolo unde exista deja dovezi solide – transplant HSC, reconstructii epiteliale, proceduri oculare specifice – calea este clara si ghidata de standarde. In alte zone, combinatia cu biomateriale si instrumente de livrare tintita, impreuna cu designuri solide de studii clinice, sunt urmatorii pasi catre validare. Actorii cheie – cercetatori, clinicieni, reglementatori si pacienti – lucreaza tot mai mult pe o matrice comuna de date, unde cifrele, nu promisiunile, decid viitorul terapiilor regenerative.